Trifenylfosfiet
Uiterlijk
| Trifenylfosfiet | ||||
|---|---|---|---|---|
| Structuurformule en molecuulmodel | ||||
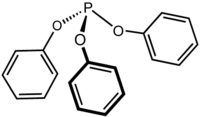
| ||||
Structuurformule van trifenylfosfiet
| ||||
| Algemeen | ||||
| Molecuulformule | C18H15O3P | |||
| Molmassa | 310,29 g/mol | |||
| CAS-nummer | 101-02-0 | |||
| EG-nummer | 202-908-4 | |||
| PubChem | 7540 | |||
| Wikidata | Q222290 | |||
| Beschrijving | Kleurloze vaste stof of heldere vloeistof met fenolachtige geur | |||
| Waarschuwingen en veiligheidsmaatregelen | ||||
| ||||
| H-zinnen | H315 - H319 - H400 - H410 | |||
| EUH-zinnen | geen | |||
| P-zinnen | P264 - P280 - P302+P352 - P321 - P332+P313 - P362 | |||
| EG-Index-nummer | 015-105-00-7 | |||
| LD50 (ratten) | 1600 mg/kg | |||
| Fysische eigenschappen | ||||
| Aggregatietoestand | vloeibaar | |||
| Dichtheid | 1,18 g/cm³ | |||
| Smeltpunt | ca. 23 °C | |||
| Kookpunt | (ontleedt) 360 °C | |||
| Onoplosbaar in | water (ontleedt langzaam) | |||
| Tenzij anders vermeld zijn standaardomstandigheden gebruikt (298,15 K of 25 °C, 1 bar). | ||||
| ||||
Trifenylfosfiet is de ester van fosfonzuur (H3PO3) en fenol. De chemische formule ervan, P(OC6H5)3, wordt vaak verkort weergegeven als P(OPh)3, waarbij Ph een fenylgroep voorstelt. Het smeltpunt van de stof ligt ongeveer bij kamertemperatuur.
Synthese[bewerken | brontekst bewerken]
Het wordt gevormd door de reactie van fosfortrichloride met fenol:
Toepassingen[bewerken | brontekst bewerken]
- Antioxidant en chelatiemiddel (metaalcomplexvormer) in polymeren en synthetische rubbers;[1] verdunningsmiddel (diluent) voor verven.
- Intermediaire stof, o.m. voor bepaalde pesticiden, farmaceutische stoffen en vlamvertragers, bijvoorbeeld tetrafenylethaan-1,2-difosfonaat, gevormd door de reactie van trifenylfosfiet met ethyleenglycol:[2]
- De reactie met methylmagnesiumbromide vormt trimethylfosfine:
Eigenschappen[bewerken | brontekst bewerken]
Trifenylfosfiet is een stof die huid en ogen irriteert en contact met de stof kan leiden tot eczeem. Blootstelling aan trifenylfosfiet kan het centraal zenuwstelsel aantasten.[3]
De stof is zeer giftig voor waterorganismen. Ze ontleedt langzaam in water.
Externe links[bewerken | brontekst bewerken]
Bronnen, noten en/of referenties
|





