Digallaan
| Digallaan | ||||
|---|---|---|---|---|
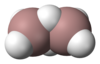
| Structuurformule en molecuulmodel | ||||
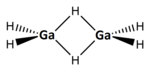
| ||||

| ||||
| ||||
| Algemeen | ||||
| Molecuulformule | ||||
| IUPAC-naam | digallaan(6) | |||
| Andere namen | Di-μ-hydrido-tetrahydridodigallium Dimeer van gallaan | |||
| Molmassa | 145,494 g/mol | |||
| SMILES | [GaH2]1[H] [GaH2] [H]1
| |||
| CAS-nummer | 12140-58-8 | |||
| Wikidata | Q516785 | |||
| Beschrijving | Witte, vaste stof Kleurloos gas | |||
| Fysische eigenschappen | ||||
| Kookpunt | ontleed | |||
| Sublimatiepunt | −50 °C | |||
| Oplosbaarheid in water | ontleed | |||
| Tenzij anders vermeld zijn standaardomstandigheden gebruikt (298,15 K of 25 °C, 1 bar). | ||||
| ||||
Digallaan is een anorganische chemische verbinding met de formule , wat ook wel genoteerd wordt, met meer nadruk op de structuur van de verbinding, als of (de μ geeft aan dat de twee waterstofatomen gebonden zijn aan beide gallium-atomen). Digallaan is het dimeer van gallaan . De uiteindelijke synthese is in 1998 voor het eerst beschreven als een chemische "tour de force",[1][2][3] hoewel later werk van Greenwood en anderen dat niet kon bevestigen.[4] Digallaan is voor het eerst in 1941 beschreven.[5] De verbinding is een kleurloos gas dat bij 0 °C ontleedt.
Synthese[bewerken | brontekst bewerken]
Digallaan is ten opzichte van gallaan stabieler, het zelfde geldt ook voor de verbindingen die bij de synthese betrokken zijn. De synthese van gallaan verloopt in twee stappen.
- In de eerste stap wordt monochloorgallaan gemaakt uit gallium(III)chloride, eigenlijk , en trimethylsilaan. In het monochloride vormen de twee chlooratomen de bruggen tussen de gallium-centra:
- Net als in digallaan zelf geeft de "μ" aan dat de chlooratomen aan beide gallium-atomen gebonden zijn.
- De tweede stap is de oplosmiddelvrije reactie bij −23 °C van het in de vorige stap gevormde monochloorgallaan met lithiumtetrahydrogallaat waarbij, zij het in lage opbrengst, digallaan ontstaat.
Onder de reactiecondities is digallaan een gas, maar bij −50 °C rijpt het tot een witte vaste stof.
Bij opwarmen tot 0 °C ontleed de stof in zijn elementen:
Structuur[bewerken | brontekst bewerken]
Elektronendiffractie van de damp bij 255 K ( ≈ −18 °C) toonde aan dat in de gasfase de structuur van digallaan vergelijkbaar is met die van diboraan: twee -groepen worden aan elkaar gekoppeld door twee waterstof-atomen in een 3-centra-2-elektronbinding.[2]. De afstand van de eindstandige (of ook wel terminale) waterstof-atomen tot gallium is 158 pm, de bruggende waterstof-atomen hebben een afstand van 171 pm tot beide gallium-atomen. De Ga-H-Ga-hoek is 98°. Het Proton-NMR van digallaan in tolueen laat twee duidelijke signalen zien, die op basis van hun intensiteit eenvoudig zijn toe te wijzen aan de eindstandige of bruggende waterstofatomen.[2]
In de vaste fase blijk digallaan een oligo- of polymere structuur aan te nemen. Het elektronendiffractiespectrum is in overeenstemming met eenheden van vier -groepen.[2] Uit het spectrum is ook af te leiden dat er eindstandge waterstofatomen aanwezig zijn, dit in tegenstelling tot aluminiumhydride (of allaan) waarin alle waterstof-atomen een bruggende functie hebben.
Dit artikel of een eerdere versie ervan is een (gedeeltelijke) vertaling van het artikel Digallane op de Engelstalige Wikipedia, dat onder de licentie Creative Commons Naamsvermelding/Gelijk delen valt. Zie de bewerkingsgeschiedenis aldaar.
- ↑ Anthony J. Downs, Michael J. Goode, Colin R. Pulham (1989). Gallane at last!. Journal of the American Chemical Society 111 (5): 1936–1937. DOI: 10.1021/ja00187a090.
- ↑ a b c d Pulham C.R., Downs A.J., Goode M.J (1991). Gallane: Synthesis, Physical and Chemical Properties, and Structure of the Gaseous Molecule Ga2H6 As Determined by Electron Diffraction. Journal of the American Chemical Society 113 (14): 5149–5162. DOI: 10.1021/ja00014a003.
- ↑ N.N. Greenwood (2001). Main group element chemistry at the millennium. J. Chem. Soc., Dalton Trans. (14): 2055–2066. DOI: 10.1039/b103917m.
- ↑ Shriver, D. F., Parry, R. W., Greenwood, N. N. (1963). Some Observations Relative to Digallane. Inorg. Chem. 2 (4): 867–868. DOI: 10.1021/ic50008a053.
- ↑ Wiberg E., Johannsen T., (1941). Über einen flüchtigen Galliumwasserstoff der Formel Ga2H6 und sein Tetramethylderivat. Naturwissenschaften 29 (21): 320. DOI: 10.1007/BF01479551.









![{\displaystyle {\ce {Ga2H6 ->[{\ce {0 \ ^{o}C}}] 2 Ga2 \ + \ 3 H2}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/a245e90bfa85eeafe095a73809bdb6ebb0ba9966)

