Gilman-reagens

De Gilman-reagentia vormen een groep van organische lithium-koperverbinding, met als algemene formule R2CuLi, waarbij R voor een alkyl- of arylgroep staat. Vanuit organisch-synthetisch oogpunt zijn dit belangrijke verbindingen omdat ze in staat zijn in organische halogeniden (organische verbindingen van chloor, broom en jood) het halogenide te vervangen door de R-groep. Vooral bij het opbouwen van grotere moleculen uit kleinere fragmenten is dit een belangrijke reactie.[1]
De reagentia zijn voor het eerst beschreven in 1952 door Henry Gilman.[2]
Toepassingen en eigenschappen[bewerken | brontekst bewerken]
Lithiumdimethylkoper kan bereid worden door koper(I)jodide in THF toe te voegen aan methyllithium bij −78 °C. In het voorbeeld hieronder wordt het Gilmanreagens ingezet om een acetyleen te methyleren.[3] De negatieve lading wordt vervolgens afgevangen via een nucleofiele acylsubstitutie op de ester, waarbij een cyclisch enon ontstaat.
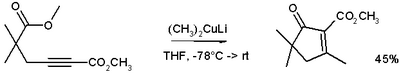
Gilman-reagentia hebben gecompliceerde structuren, zowel in kristallijne vorm als in oplossingen. Lithiumdimethylkoper is een dimeer in di-ethylether, waarbij een 8-ring gevormd wordt met twee lithiumatomen die beiden door twee methylgroepen worden gecoördineerd. Op dezelfde wijze vormt lithiumdifenylkoper in vaste toestand een dimeer ethercomplex.[4]

Als interactie met de Li+-ionen geblokkeerd wordt door complexatie ervan met een kroonether, met name 12-kroon-4, dan vormen de losse dialkylkoper-anionen die overblijven een lineaire structuur rond het koperatoom.[5]
Zie ook[bewerken | brontekst bewerken]
Externe links[bewerken | brontekst bewerken]
Bronnen, noten en/of referenties
|
